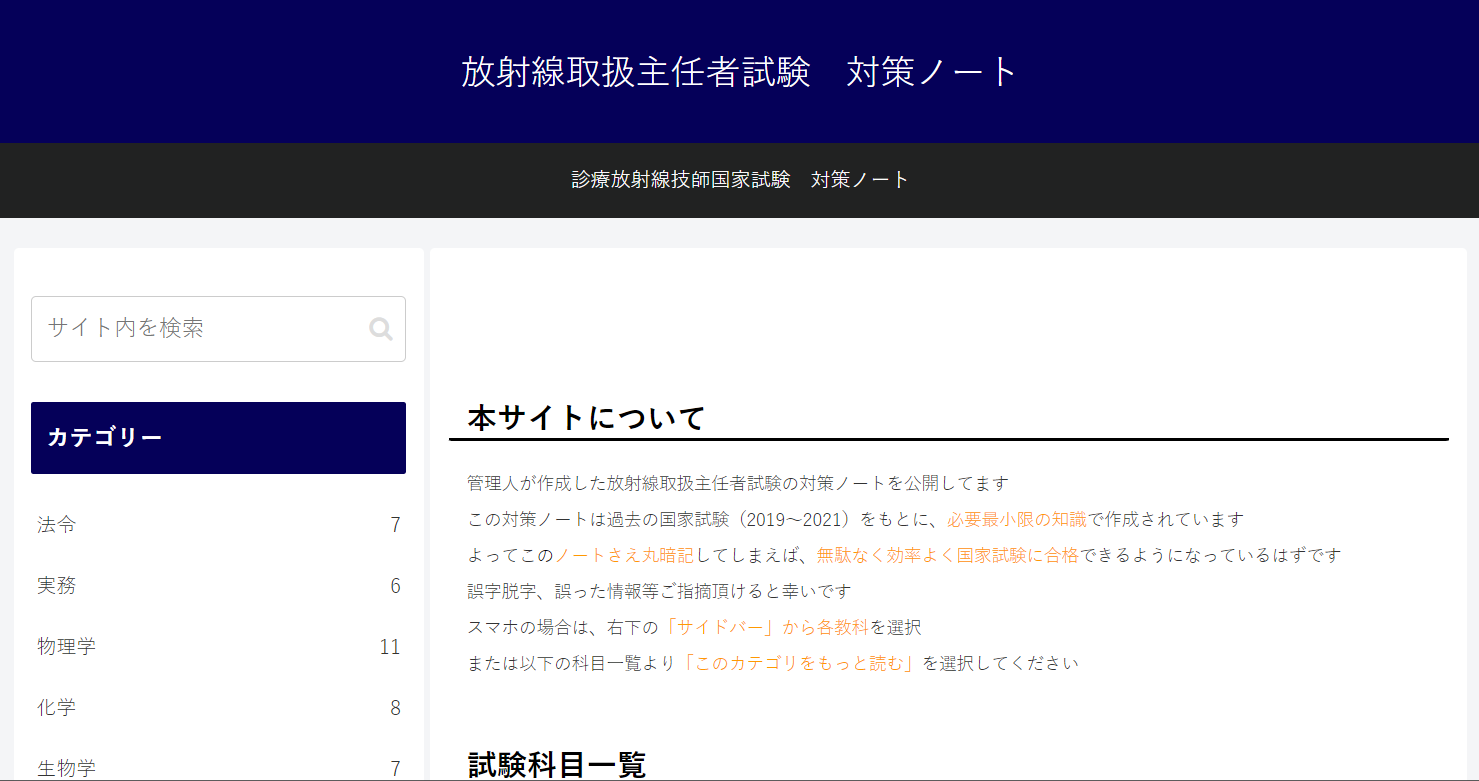
放射性核種
核種まとめ (R4.1.4(実務), R4.12(物理), R4.2.11.31, R3.8(物理), R3.1(実務), R3.10.12.18, R2.28,R1.15.17.27) 核種 壊変 方式 エネルギー(MeV) α・β線 γ線 半減期 その他 3H★ β- 0.02 12年 β線のみ放出/天然RI/ 7Be★ EC 0.5 53日 中性子線源/天然RI 11C β+ 0.511 20分 14N(p,α)11C 14C★ β- 0.15 5.7×103年 β線のみ放出/天然RI 13N β+ 0.511 10分 16O(p,α)13N 15O β+ 0.511 2分 14N(d,n)15O 18F β+ 0.511 110分 20Ne(d,α)18F 18O(p,n)18F 30P★ β+ 0.511 2.5分 初めて人工的に得られたRI 32P★ β- 1.7 14日 β線のみ放出 35S★ β- 0.17 87.5日 低エネルギーβ線 40K★ β- 1.3 1.2×109年 天然RI/12億年 45Ca★ β- 0.26 ...
放射性壊変と放射能 / 核分裂
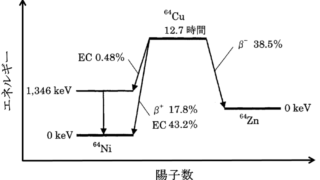
放射性壊変と放射能 (R5.5, R4.1.4.13, R3.14(生物), R3.19, R1.2.3.4) ・放射能A A = -dN/dt = λ×N ・壊変定数λ λ = loge2/T = 0.693/T T:半減期 ・原子数N (R5.1.3, R4.2(実務), R3.4) N = w/W×6.02×1023 w:放射性物質の質量 W:対象物質の原子量 w/W:モル数 6.02×1023:アボガドロ定数 ・分岐比 (R2.1,R1.2.7(物理)) λ=λ1+λ2+λ3+…… λ1,λ2,λ3:部分半減期 分岐比 → λ1:λ2=T2:T1 ・平均寿命τ τ=1/λ=1.44×T ・壊変図 (R4.17) 放射性壊変の方法に関してはこちら↓ 「対策ノート:放射性壊変」 放射線計測で得られる計数 (R1.5(物理)) ・t0からt秒までの壊変数T T=N×(1-e-λt) = A0/λ×(1-e-λt) A0,N0:t0の時の放射能,原子数 ・t秒計測したときの検出される確率p p=ε×(1-e-λt) ε:検出効率 自発核分裂...

放射平衡
放射平衡 (R4.5, R3.2, R1.6.7.8) ・過渡平衡 (R5.8, R3.3.4) 成立条件:λ1<λ2,T1>T2 時間経過によって A2>A1,T2→T1となる ・永続平衡 (R5.4(物理), R3.14) 成立条件:λ1<<λ2,T1>>T2 時間経過によって A2=A1,T2→T1となる ・平衡になる核種の例 (R5.7) ・68Ge-68Ga(永続平衡) (270d-68m) ・82Sr-82Rb (25d-1.2m) ・81Rb-81mKr (4.6h-13s) ・83Rb-83mKr (86d-1.8h) ・87Y-87mSr (80h-2.8h) ・90Sr-90Y(永続平衡)★ (29y-64h) ・90Mo-99mTc(過渡平衡) (66h-6h) ・113Sn-113mIn (115d-1.6h) ・132Te-132I (77h-2.3h) ・137Cs-137mBa(永続平衡) (30y-2.5m) ・140Ba-140La(過渡平衡) (12.8d-1.68d) ・226Ra-222Rn(永続平衡) ...

核反応とRI製造
核反応式 (R5.9.10, R5.1(物理), R4.7.9.10, R3.6, R2.10(物理), R2.8, R1.9.10.11) A(x,y)B A:標的原子核 x:入射粒子 y:放出粒子 B:反跳原子核 (A+x)と(B+y)の陽子と中性子の数, エネルギーは等しい Q値 (R5.9(物理), R4.1(実務), R3.14(物理), R2.11.12(物理),R1.10(物理)) 核反応前後の質量欠損をエネルギーに換算した値 Q = (MA+Mx)×C2-(MB+My)×C2 ・発熱反応 :Q値>0 閾エネルギーはない ・吸熱反応 :Q値<0 閾エネルギーはある 入射粒子が閾値以上のエネルギーを持っている必要がある ≒入射粒子にエネルギーが必要なので発熱反応より起こりずらい反応 代表的な吸熱反応を以下に示す 32S(n,p)32P 27Al(n,α)24Na ・閾値Emin Emin= -Q×(MA+Mx)÷MA 標識化合物の分類 (R3.20) ・特定(S)標識化合物 標識位置が明らかな場合(95%以上) ・名目(N)標識化合物 標...
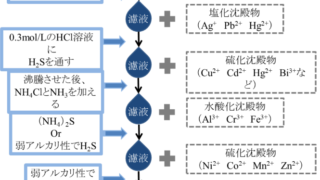
RIの分離法
共沈法 (R5.22.31, R3.4(実務), R3.26, R2.5,R1.31) ・同位体担体 :必要なRIの安定同位体の担体 ・非同位体担体 :不必要なRIの安定同位体の担体 ・スカベンジャー :不必要なRIを沈殿させるための担体 ・保持担体 :必要なRIを溶液に留めるための担体 ・捕集剤 :必要なRIを沈殿させるための担体 ・溶解度積 共沈法では溶解度積の小さい反応が選ばれる 溶解度積=「溶解した塩の濃度」×「溶解しなかった塩の濃度」 ・共沈法の実例 (R4.4(実務), R3.32, R2.22.32) 溶液中のRI 捕集剤 保持担体 沈殿物 140Laと140Ba Fe3+ Ba2+ 140La 90Yと90Sr Fe3+ Sr2+ 90Y 32Sと32P Fe3+ SO42- 32P *沈殿物は分離後,溶媒抽出することで無担体にできる ・担体の条件 化学的に安定したもので、目的操作を阻害しない 目的物質と同様の挙動を示す必要がある 化学反応の詳細はこちら↓ 「対策ノート:化学反応」 溶媒抽出法 (R5.31, R4.25, R3.32, R2.23) 分離が(...

放射化分析
放射化分析の利点 「検出感度が良い」 「試薬などの汚染がない」 「核反応なので元素の化学的性質に影響されない」 「多元素同時分析ができる」 「非破壊分析ができる」 放射化分析の欠点 「精度が低い」 「副反応による妨害がある」 「自己遮蔽の影響がある」 「原子炉など中性子発生源が必要」 生成放射能の計算 (R5.32, R4.6, R3.7.31, R2.7.3(実務),R1.31.32) ・試料を時間t照射して,直後に得られる放射能A A=f×σ×N×(1-e-λt) =f×σ×N×(1-(1/2)t/T) f:照射粒子束密度(n/cm2・s) σ:放射化断面積 N:試料の原子数 ・原子数N N=θm/M ×6.02×1023 θ:存在比 m:試料質量 M:試料原子量 また,t<<Tの場合 A = f×σ×N×(0.693×t/T) ・照射終了後,時間d経過後の放射能Ad Ad=A×e-λd =A×(1/2)d/T 放射化分析 (R5.26) ・放射線計測 「Ge(Li)」または「Ge」半導体検出器つき多重波高分析器を使用する →γ線に対するエネ...

RIの化学分析への利用
年代測定 (R5.18, R4.16, R2.18.27) ・炭素14法 :14C →14N,14C/12Cの割合を測定する 生物(死骸)に適用 ・カリウム-アルゴン法 :40K→40Arの量を測定する 鉱物に適用 ・アルゴン-アルゴン法 :40Arと中性子照射してできた39Arの比を求める 鉱物に適用 ・ウラン-鉛法 :238U→206Pbと235U→207Pbの比を測定する 鉱物に適用 ・フィッショントラック法 :238Uの自発核分裂による飛程の密度とウラン量から求める 鉱物に適用 オートラジオグラフィ (R3.32, R1.25(物理)) イメージングプレート等を用いてRIの分布を可視化する 基本的な性能としてIP法>写真(フィルム)法 ミクロオートラジオグラフィでは低エネルギーγ線が適する 直接希釈法 (R5.25, R3.24, R2.26,R1.25) 目的物質が非放射性で,加える同位体が放射性である分析法 重量 比放射能 全放射能 添加前 目的の試料 X 0 トレーサ(RI) a S0=A/a A 添加後 混合物 X+a S=A/w...
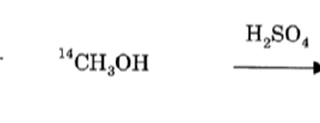
化学反応
化学:(R5.20, R4.12.19.21, R3.15.16, R2.21.24,R1. 5.18.20.21) 実務:(R4.4, R2.4,R1.4) 沈殿発生系 ・硫酸塩沈殿X SO4 ↓ X:「Ca2+」「Sr2+」「Ba2+」「Pb2+」「2Ag+」 ・リン酸塩沈殿 ( X ) + HPO42- → X HPO4 ↓ 3( X ) + 2OH- + 2HPO42- → X3 (PO4)2 ↓ + 2 H2O X:「Ca2+」「Sr2+」「Ba2+」 ( X ) +PO43- → X PO4↓ X:「Fe3+」「3Ag+」「Al3+」 ・硫化物沈殿しないもの X S↓ 「Mg2+」「Ca2+」「Sr2+」「Ba2+」「Na2+」「K2+」「Cs2+」 ・塩化物沈殿 X Cl↓ X:「Hg+」「1/2Pb2+」「Ag+」 ・クロム酸塩沈殿 X CrO4↓ X:「Ba2+」「Pb2+」「2Ag+」 ・炭酸塩沈殿X CO3↓ X:「Ba2+」「Sr2+」「2Ag+」「Ca2+」 気体発生系 FeS+2HCl → FeCl2+H2S↑ NaHCO3+HCl → NaCl+H2O...
放射線と化学についての範囲
出題範囲が物理と被りやすいので、対策ノートではどちらかに記載してあるはず
記事検索を使っていただけると探しやすい
出題方式としては選択問題30問30点、文章問題大門2問30点の計60点
放射線主任者の問題としては結構直球に「ザ・放射線」みたいな内容なのでできるだけ得意科目にしたい
出題範囲の一つにRIほぼ関係なく、化学反応式を覚えてなくてはならない問題があるので、中学化学程度でいいがまとめて覚えておくとよい
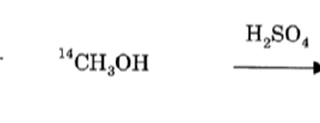
化学反応
化学:(R5.20, R4.12.19.21, R3.15.16, R2.21.24,R1. 5.18.20.21) 実務:(R4.4, R2.4,R1.4) 沈殿発生系 ・硫酸塩沈殿X SO4 ↓ X:「Ca2+」「Sr2+」「Ba2+」「Pb2+」「2Ag+」 ・リン酸塩沈殿 ( X ) + HPO42- → X HPO4 ↓ 3( X ) + 2OH- + 2HPO42- → X3 (PO4)2 ↓ + 2 H2O X:「Ca2+」「Sr2+」「Ba2+」 ( X ) +PO43- → X PO4↓ X:「Fe3+」「3Ag+」「Al3+」 ・硫化物沈殿しないもの X S↓ 「Mg2+」「Ca2+」「Sr2+」「Ba2+」「Na2+」「K2+」「Cs2+」 ・塩化物沈殿 X Cl↓ X:「Hg+」「1/2Pb2+」「Ag+」 ・クロム酸塩沈殿 X CrO4↓ X:「Ba2+」「Pb2+」「2Ag+」 ・炭酸塩沈殿X CO3↓ X:「Ba2+」「Sr2+」「2Ag+」「Ca2+」 気体発生系 FeS+2HCl → FeCl2+H2S↑ NaHCO3+HCl → NaCl+H2O...